【背景】
为了追逐高能量密度的电池系统,金属锂负极已经被研究了几十年,因为其高理论比容量和低还原电位。然而,几乎所有可充电的锂金属电池都存在枝晶生长的问题,并大大阻碍了其实际应用。严重的枝晶生长使部分锂从集流体中分离出来,成为死锂,这将导致安全问题和电池的快速衰减。通过电解质优化、稳定的界面结构、先进的结构设计和电池工作条件的调节,在无枝晶金属锂负极方面已经取得了深入的进展。然而,大多数策略的目的是减少枝晶物的形成,但很少有工作专注于如何解决已经形成的锂枝晶物和衍生的死锂。死锂是一个严重的副产物,因为它会导致容量衰减、寿命不足和热失控。重新激活死锂是解决上述问题的一个有吸引力的方法,因为它可以减缓锂的消耗并改善界面的稳定性。这种方法更侧重于解决现有的副产物,而不是放慢产生速度,以便它可能保持长期的有效性。
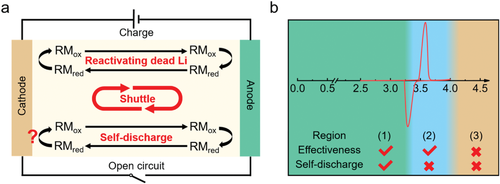
图1 a) 重新激活死锂的循环反应和由氧化还原介质穿梭产生的自放电的示意图。b) LiFePO4 (LFP)正极的典型循环伏安法(CV)曲线和由氧化还原介质的氧化还原电位划分的三个区域。
Tao的研究小组提出了一种新的锂修复方法,以三碘/碘化物(I3− /I− )氧化还原对为媒介,使死锂恢复活力,补偿锂的损失。在充电过程中,氧化的氧化介质(RMox , I3− )与死锂自发反应,变成还原的氧化介质(RMred , I− )和Li+ 。然后RMred 扩散到正极一侧,并失去电子再次被氧化成RMox。这样,只要氧化剂在正极一侧能够被氧化,死锂就可以通过氧化剂的穿梭而不断地被重新激活(图1a)。事实证明,这种策略非常成功,只需使用非常有限的锂作为负极,就能实现优秀的电池性能。实际上,有限的锂源对于实用的金属锂电池来说是至关重要的,当负极与正极容量比(N/P比)增加时,比能量急剧下降。死锂的有效再活化使其在低N/P比下更容易实现更好的电化学性能。此外,在电池中引入氧化还原剂是很容易实现的,而且也能与其他锂金属负极改性策略兼容。然而,以前的工作发现I3− /I−氧化还原介质在电池保持充电状态时引起严重的自放电。如图1a所示,由于锂金属的强还原性,无论电池处于何种状态,RMox都不可避免地转化为RMred。然后,如果氧化的正极材料能够与RMred 反应并再次生成RMox,循环反应将持续进行,这导致了自放电。
我们提出,用于重新激活锂金属电池中死锂的氧化还原剂的选择原则,即氧化还原剂的氧化还原电位应低于充电截止电压,以确保重新激活死锂的循环反应。同时,它也应该高于正极材料的氧化还原电位,以避免自放电的循环反应。为了阐明选择原则,作我们以二茂铁(Fc)、10-甲基吩噻嗪(MPT)和噻蒽(Th)这三种氧化还原剂为例。它们与空白组在重新激活死锂和自放电方面进行了比较,在LiFePO4 |Cu无负极锂金属电池中。根据选择原理的预测,MPT是一种合适的氧化还原介质,它被证实能有效地重新激活死锂,并在充电状态下静置3天后保持高容量。此外,2,2,6,6-四甲基哌啶氧基(TEMPO)作为选择原则的延伸,也被证明是一种合适的氧化还原介质。
【具体内容】
据报道,具有有序橄榄石结构的LiFePO4 |Cu全电池可产生3.4V(vs. Li/Li+)的稳定电位,因此选择LiFePO4正极来验证该原理。而图1b中LFP|Cu全电池的循环伏安法(CV)曲线也证实了这一点。根据选择原则,电压范围被分为三个区域。(1)低于LFP(正极)的氧化还原电位,ERM(氧化还原介质的氧化还原电位)< ELFP;(2)在LFP的氧化还原电位和全电池的电荷截止电压之间,ELFP < ERM < EOFF (全电池的截止电位);(3)高于全电池的电荷截止电压,EOFF < ERM 。重新激活死锂的有效性和自放电是两个主要的调查点。如果氧化还原剂的氧化还原电位位于区域(1),氧化还原剂可以通过带电的正极材料或正极化的集流体被氧化,这意味着氧化还原剂可以有效地重新激活死锂,但带来严重的自放电行为。位于区域(2)代表氧化还原剂只能通过正极化的集流体被氧化,这意味着有效地重新激活死锂,几乎没有自放电。如果氧化还原剂位于区域(3),甚至不能被氧化,对相应的全电池没有任何影响。
Fc、MPT和Th已被发现是电池环境中有效的氧化还原介质。图2a中相应的CV曲线显示Fc的氧化峰在3.3V左右,MPT在3.6V左右,Th在4.1V左右,所以它们是三个典型的介体,分别位于(1)、(2)和(3)区域。电流密度影响极化,并使氧化还原反应的氧化峰发生移动。在充电过程中,电流密度的增加会使氧化峰转移到高电位。然而,在CV测试中,Fc的氧化峰在3.3V左右,MPT在3.6V。在普通的电流密度下,氧化峰通常不会移到4V以上,所以氧化还原剂仍然可以被氧化,以重新激活死锂。图2b中提供了结构公式和与Li+/Li的可逆反应。不同的添加剂在纽扣电池测试中被进一步评估。正如文献中所报道的。氧化还原剂在电极间可承载的极限电流为
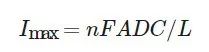
(n:氧化还原剂携带的基本电荷数,F:法拉第数,A:平面电极的面积,D:氧化还原剂的扩散系数,C:氧化还原剂的浓度,L:电极的间距)。F、A和L是固定的,而n和D是特定氧化还原剂的常数。因此,氧化还原剂的浓度影响着极限电流和穿梭效应。
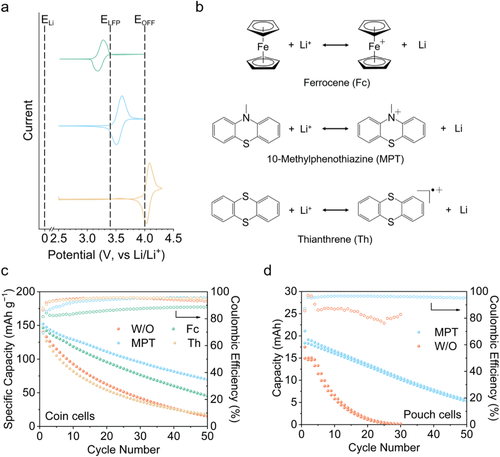
图2 a)二茂铁、10-甲基吩噻嗪和噻蒽在0.01 mV s–1的扫描速率下的循环伏安法(CV)曲线,b)它们的结构式和与Li+ /Li的可逆反应。含有不同添加剂的LiFePO4 (LFP)|Cu全电池的长期循环性能c)在纽扣电池中和d)在软包电池中。
图2c显示了使用不同添加剂的纽扣电池的循环性能。不加添加剂的LFP|Cu全电池在第二个循环时显示出133.1 mAh g−1 的比放电容量,并在50个循环后仅保持15.2mAh g−1的容量。当添加添加剂时,第二个周期的具体放电容量变为:Fc添加剂为142.2 mAh g−1 ,MPT添加剂为147.5 mAh g−1,Th添加剂为127.0 mAh g−1。这表明重新激活死锂的添加剂甚至可以在最初的几个循环中发挥作用。50次循环后,Fc添加剂的容量为45.3mAh g−1,MPT添加剂为69.9 mAh g−1,Th添加剂为17.6mAh g−1,这意味着Fc和MPT添加剂是有效的,但Th添加剂对重新激活死锂没有影响。由于MPT添加剂在纽扣电池中的性能最好,所以进一步制造了软包电池来评估MPT添加剂的效果。如图2d所示,没有添加剂的软包电池在第二个循环中显示出14.6 mA h的放电容量,并在30个循环中失去了几乎所有的容量。相比之下,当加入MPT添加剂时,软包电池在第二个周期显示出18.3mA h的放电容量,并在50个周期后保持5.3mA h的容量。由于压力低、容量大等原因,软包电池通常伴随着较差的电化学性能。然而,MPT添加剂在软包电池中仍然表现出突出的性能,这进一步验证了重新激活死锂的有效性。
有无MPT添加剂的LFP|Cu全电池在五个循环后被拆开,进行锂形态表征。图3显示了铜箔上锂沉积的数码照片和相应的扫描电子显微镜(SEM)图像,这些图像来自于不加添加剂的LFP|Cu电池在完全充电和放电状态下获得。当没有添加剂时,照片中铜箔上沉积的锂是黑色的,显示出粗糙的形态。相比之下,当使用MPT添加剂时,它似乎更有光泽和紧凑(图3c)。横截面SEM图像也显示出与图3a,c中的照片相同的特征。与图3b相比,图3d的照片和SEM图像中的残留物也较少。这些结果证明了MPT添加剂在循环过程中保持良好的锂形态和减少死锂的有效性。

图3从LiFePO4 (LFP)|Cu纽扣电池(a,b)不加或(c,d)加10-methylphenothiazine (MPT)添加剂得到的铜箔上锂沉积的横截面扫描电子显微镜(SEM)图像和相应的数字照片。LFP|Cu比色皿式全电池(e-i)在没有或(j-n)有MPT添加剂的情况下,充电电流为1mA时,充电过程中的锂沉积的光学观察。
图3e-h显示了在充电电流为1mA的LFP|Cu全电池的充电过程中,锂-铜负极界面的演变。在基础电解液中仅沉积了10分钟后,就在负极界面上观察到明显的枝晶物。然后在20分钟(图3g)和30分钟(图3h)后,苔藓状的树突急剧增长。如比色皿式电池的数码照片所示(图3i),树突最后甚至成了宏观的。在相同的条件下,对含有MPT添加剂的电解液中的锂沉积观察进行了处理。可以看出,在整个过程中,锂的沉积形态是光滑的,基本上没有枝晶物,而且可以清楚地观察到密集的锂沉积层,如图3j-m所示。此外,在数字照片中没有发现锂沉积后的枝晶物(图3n)。众所周知,比色皿式电池对锂负极是不利的,因为在这种电池中没有对沉积的锂施加压力。视觉上的鲜明对比表明,MPT添加剂确实可以与枝晶物和死锂反应,并有助于建立一个稳定的界面。
对于间接电化学性能和锂沉积形态的表征,需要一个量化的指标来证明添加剂和死锂之间的连续反应。如图4a所示,设计的电池使用不锈钢(SS)箔正电极,面对循环的锂-铜箔作为负电极。在完全充电的状态下,从循环的LFP|Cu全电池上拆下Li-Cu负极,并加入不同添加剂的电解液进行测试。然后施加3.8V的恒定电压60分钟,并记录响应电流,如图4b所示。该实验旨在模拟LFP|Cu全电池的充电过程,因此需要一个外加电压来氧化氧化还原介质。该电压应高于MPT的氧化还原电位,但低于Th的氧化还原电位。此外,LFP|Cu电池的截止电压通常设定在3.8-4.0V之间。因此,电压最终设定为3.8V。添加剂首先与枝晶的Li和死Li发生自发反应,然后如果RMred 能在3.8V的恒定电压下在正极被氧化成RMox ,重新激活死Li的循环反应就建立了。在氧化过程中,电子将通过外部电路转移,并产生响应电流。因此,这项工作中的量化指标是响应电流,它可以代表重新激活死锂的循环反应。可以看出,基础电解液和Th添加剂的响应电流几乎为0,这意味着这些电池在3.8V下没有循环反应。但Fc和MPT添加剂的响应电流稳定在0.1mA左右。在这些电池中肯定发生了重新激活死锂的连续循环反应。此外,在测试后,电池被拆开,并将锂-铜负极与初始状态下的负极进行比较。如图4c所示,循环的锂-铜箔在使用前是均匀的。在基础电解液或含Th的电解液中测试后,没有观察到明显的变化。然而,当采用Fc和MPT时,黑色的锂沉积在一定程度上变成了闪亮的,因为在这个过程中一些枝晶和死锂被消耗了。电流反应和相应的形态变化相结合,证实了在使用适当的添加剂时存在重新激活死锂的循环反应。这里适当的添加剂(Fc和MPT)应该拥有低于电荷截止电压(3.8-4.0V)的氧化还原电位。
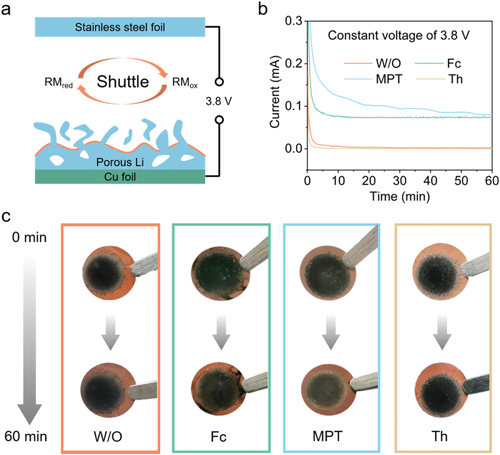
图4 a) 所设计的SS|Li-Cu全电池的示意图。b) 恒定电压为3.8V的SS|Li-Cu全电池的响应电流曲线。c) 测试前后Li-Cu负极的数码照片对比。
根据本工作的选择原则,添加剂是否会引起严重的自放电行为是另一个标准。使用不同电解质的LFP|Cu全电池循环10次,并在完全充电状态下保持3天,然后继续进行循环程序。图5a-h分别显示了四个电池在第9、10、11个循环时的充放电曲线和电压-时间曲线。在静止时间内会损失一定量的容量,所以容量保持率被用来衡量自放电的程度。经计算,基础电解液的容量保持率为90.5%,Fc添加剂为0.0%,MPT添加剂为85.8%,Th添加剂为92.9%(图5i)。自放电测试在充电过程结束后立即开始。MPT氧化还原剂在这种状态下被氧化,由于金属锂的强还原性,它将不可避免地与沉积的锂发生反应。部分金属锂被消耗掉,在自放电测试后,放电容量减少。所以有MPT的容量保持率比没有任何添加剂的容量保持率要低一点,而且降低的程度取决于MPT添加剂的数量。然而,被还原的MPT不会再被带电的正极材料氧化,所以自放电不会发生。带有Fc添加剂的电池的开路电压在自放电测试后甚至下降到2V以下(图5d),而其他电池的电压保持在3.4V以上。结果表明,添加Fc后发生了严重的自放电。在进行了同样程序的自放电测试后,其他全电池被拆开以进一步验证自放电。图5j所示,正极显示出最明显的XRD图案,对应于LiFePO4 (PDF#40-1499),当使用Fc添加剂时,只有一个铜箔有少量的残留物,而其他的是铜箔有一层Li沉积。在使用空白电解液或使用Th添加剂的电池中,锂的沉积是粗糙的,而在MPT添加剂的作用下,锂的形态变得平滑。然而,在使用Fc添加剂的电池中,几乎没有观察到锂的沉积,并且铜箔被暴露出来。沉积的锂在放电过程中全部消耗掉了。为了评估自放电行为对后续循环的影响,通过比较第9次和第11次循环时的容量得到了容量恢复。经计算,基础电解液的容量恢复率为90.7%,Fc添加剂为91.8%,MPT添加剂为94.7%,Th添加剂为90.8%,这意味着无论是否发生严重的自放电行为,它们都能完全恢复。事实上,只有当氧化还原剂在开路情况下能被正极材料氧化时,自放电行为才会发生,在这种情况下,自放电的循环反应才能建立。这里的添加剂(Fc)代表拥有比正极材料(LFP)的氧化还原电位低的氧化还原电位。
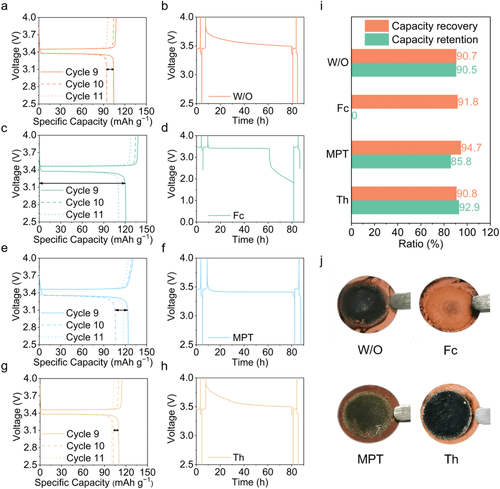
图5 LiFePO4 (LFP)|Cu全电池(a,b)在没有或加入(c,d)二茂铁(Fc)、(e,f)10-甲基吩噻嗪(MPT)和(g,h)噻蒽(Th)添加剂时的充放电曲线和电压时间曲线。i)全电池的容量保留和容量恢复的比较。j)自放电测试后Li-Cu负极的数码照片比较。
基于上述分析和验证,重新激活锂金属电池中死锂的最佳氧化还原介质应位于区域(2)(图1b),该区域代表着正极材料的氧化还原电位和全电池的充电截止电压之间的氧化还原电位。MPT添加剂已被证明能成功地重新激活死的锂,并具有很小的自放电行为。为了进一步说明选择原则的延伸,根据其氧化还原电位列出了几种可能的氧化还原介质:2'2-联吡啶和1,10-菲罗啉的铁复合物(3.8-3.9V),四氯化碳(3.76V),二茂铁甲醛(3.54 V)和TEMPO。而TEMPO在这项工作中得到了进一步评估。如图6a所示的带有TEMPO添加剂的SS|Li电池的CV曲线,TEMPO的氧化还原电位确实位于3.4-3.6 V,图6b显示了其结构式和与Li+ /Li的可逆反应。在含有50 mM TEMPO添加剂的SS-Cu全电池中,响应电流的量化指数稳定在0.1 mA左右(图6c),这证明了重新激活死锂的循环反应的存在。此外,全电池稳定地循环了50次以上,并保持了50.5 mAh g−1 的容量(图6d)。至于自放电测试,含有TEMPO添加剂的LFP|Cu全电池在第9、10和11个循环时的放电容量分别为115.1、98.7和108.2 mAh g−1 ,容量保持率为85.8%,容量恢复率为94.0%,这说明自放电行为很少,自放电的循环反应失败(图6e)。再一次验证了TEMPO添加剂成功用于氧化还原介质在金属锂电池中重新激活死锂的选择原则。
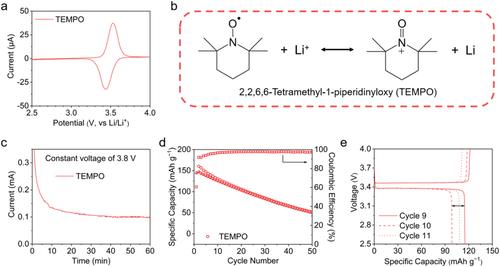
图6a) 2,2,6,6-四甲基哌啶氧化物(TEMPO)在0.01 mV s–1 的扫描速率下的循环伏安法(CV)曲线;b) 其结构式和可逆反应。c) 恒定电压为3.8 V的SS|Li-Cu全电池的响应电流曲线。d) 在纽扣电池中加入TEMPO添加剂的磷酸铁锂4 (LFP)|Cu全电池的长期循环性能。e) 加入TEMPO添加剂的LFP|Cu全电池在第9、10和11个循环的充放电曲线。
即使使用合适的氧化还原介质(MPT和TEMPO),仍然有几个缺陷。能量效率会很低,因为它需要过度充电来创造一个稳定的穿梭机制。但是,当电池中没有氧化还原介质时,由于副反应和死锂的形成,库仑效率很低,导致能源效率低和循环性能差。然而,当使用氧化还原剂时,即使需要额外的能量来氧化添加剂,死锂也可以被重新激活,循环性能得到改善。相比之下,使用氧化还原剂的方法仍然具有吸引力。另一个疑问是氧化的氧化还原介质是否能与沉积好的金属锂反应。基于化学上的考虑,该反应确实是可行的。但是,死锂和锂枝晶通常覆盖在沉积好的锂上,并且拥有大的表面积,所以氧化还原剂和死锂之间的反应更具竞争性。我们相信,在穿梭过程中,很少有沉积良好的锂会被反应。
除了氧化还原电位之外,在选择用于重新激活锂金属电池中的死锂的氧化还原介质时,还应该考虑其他因素。首先,氧化和还原的氧化还原剂应始终溶于电解质,以便产生穿梭效应。然后,氧化还原介体应该与任何电池成分没有任何副反应。最后,氧化还原媒介物携带的基本电荷数量和氧化还原媒介物的扩散系数应该相对较大,以降低氧化还原媒介物的浓度。
【结论】
提出了用于重新激活锂金属电池中死锂的氧化还原介质的选择原则,并进行了深入的验证。根据选择原则,三个区域被氧化还原剂的氧化还原电位所划分。Fc,其氧化还原电位低于正极材料的氧化还原电位,已被证明能有效地重新激活死锂,但会导致严重的自放电。MPT和TEMPO,其氧化还原电位在正极材料的氧化还原电位和全电池的截止电压之间,已被证明能成功地重新激活死锂,并具有很小的自放电行为。对于Th,其氧化还原电位高于正极材料的氧化还原电位,已被证明对电池没有影响。因此,最合适的氧化还原剂应该拥有介于正极材料的氧化还原电位和全电池的截止电压之间的氧化还原电位。这样的选择原则将激励研究人员为锂金属电池和其他电池寻找更合适的氧化还原介质。
文章链接:Selection of Redox Mediators for Reactivating Dead Li in Lithium Metal Batteries